Geïnduceerde pluripotente stamcellen (iPSC's) van patiënten bieden een ongekende mogelijkheid om menselijke ziekten te modelleren in een schaaltje. Door deze cellen te differentiëren in celtypes die relevant zijn voor ziekten, kunnen onderzoekers de moleculaire mechanismen bestuderen die ten grondslag liggen aan verschillende pathologieën en screenen op potentiële kandidaat-geneesmiddelen.
Zo zijn iPSC-afgeleide cardiomyocyten van patiënten met genetische hartaandoeningen gebruikt om ziektefenotypes na te bootsen en de werkzaamheid van therapeutische verbindingen te testen.

Er moeten echter verschillende uitdagingen worden aangepakt voordat iPSC's op grote schaal kunnen worden gebruikt voor ziektemodellering en therapie. Onderzoek is erop gericht om deze problemen aan te pakken door efficiëntere en gestandaardiseerde herprogrammeringsmethoden te ontwikkelen, differentiatieprotocollen te verfijnen en strenge kwaliteitscontrolemaatregelen te implementeren.
Vooruitgang in genbewerkingstechnologieën zoals CRISPR/Cas9 maakt het ook mogelijk om ziekteveroorzakende mutaties te corrigeren in iPSC's van patiënten, wat de weg vrijmaakt voor autologe celvervangingstherapieën.
De Rol van Stamcellen in de Regeneratieve Geneeskunde
De komst van iPSC-technologie heeft spannende mogelijkheden geopend voor de regeneratieve geneeskunde. In tegenstelling tot embryonale stamcellen, kunnen iPSC's worden afgeleid van de eigen cellen van een patiënt, waardoor ethische bezwaren en het risico van immuunafstoting worden vermeden.
Naarmate het veld zich verder ontwikkelt, zullen er naar verwachting meer klinische onderzoeken komen met iPSC-afgeleide cellen. IPSC's zijn een krachtig hulpmiddel voor het modelleren van ziekten, het ontdekken van medicijnen en regeneratieve geneeskunde. Hoewel er nog uitdagingen zijn, houden het snelle onderzoekstempo en de technologische vooruitgang op dit gebied een grote belofte in voor een revolutie in de behandeling van verschillende menselijke ziekten.
Embryonale Stamcellen (ESC's): Eigenschappen en Toepassingen
Embryonale stamcellen (ESC's) zijn pluripotente stamcellen die afkomstig zijn uit een zeer vroeg stadium van het embryo, meestal het blastocyststadium (ongeveer 4-5 dagen na de bevruchting bij mensen). Door deze bijzondere eigenschappen zijn embryonale stamcellen van groot belang in wetenschappelijk onderzoek.
Ze worden gebruikt bij het bestuderen van de vroege menselijke ontwikkeling, bijvoorbeeld om te begrijpen welke transcriptiefactoren en signaalroutes de eerste celbeslissingen aansturen.
Het gebruik van embryonale stamcellen voor onderzoek werpt echter ethische vragen op, omdat voor het verkrijgen van deze cellen een embryo wordt vernietigd. Daarom is er ook veel onderzoek naar alternatieven, zoals geïnduceerde pluripotente stamcellen (iPSC's), die uit volwassen lichaamscellen worden gemaakt maar vergelijkbare eigenschappen hebben.
Pluripotentie en Zelfvernieuwing van ESC's
Embryonale stamcellen (ESC's), afkomstig uit het blastocyststadium van vroege zoogdierembryo's, onderscheiden zich door hun vermogen om te differentiëren tot elk embryonaal celtype en door hun vermogen om zichzelf te vernieuwen. Het zijn deze eigenschappen die ze waardevol maken op wetenschappelijk en medisch gebied.
Embryonale stamcellen van de embryoblast zijn pluripotent, wat betekent dat ze kunnen differentiëren om primitief ectoderm te genereren, dat uiteindelijk tijdens de gastrulatie differentieert in alle derivaten van de drie primaire kiembladen: ectoderm, endoderm en mesoderm. Deze kiembladen genereren elk van de meer dan 400 celtypen in het volwassen menselijk lichaam.
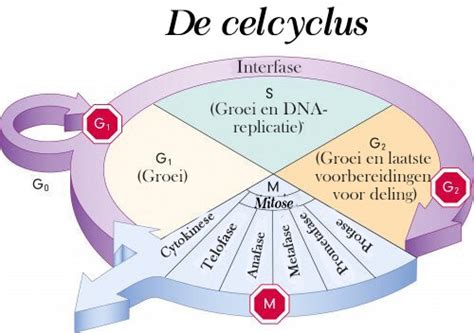
Celcyclus en Proliferatie van ESC's
Wanneer ESC's de juiste signalen krijgen, vormen ze aanvankelijk voorlopercellen die vervolgens differentiëren tot de gewenste celtypen. Onder bepaalde omstandigheden kunnen embryonale stamcellen in een ongedifferentieerde staat zichzelf onbeperkt te vernieuwen.
ESC's delen zich zeer frequent vanwege een verkorte G1-fase in hun celcyclus. Snelle celdeling zorgt ervoor dat de cellen snel in aantal toenemen, maar niet in grootte, wat belangrijk is voor de vroege embryonale ontwikkeling. In ESC's worden cycline A- en cycline E-eiwitten die betrokken zijn bij de G1/S-overgang altijd op hoge niveaus tot expressie gebracht. Cycline-afhankelijke kinases zoals CDK2 die de voortgang van de celcyclus bevorderen, zijn overactief, deels vanwege de downregulatie van hun remmers. Retinoblastoom-eiwitten die de transcriptiefactor E2F remmen totdat de cel klaar is om de S-fase in te gaan, worden in ESC's hypergefosforyleerd en geïnactiveerd, wat leidt tot voortdurende expressie van proliferatiegenen. Deze veranderingen resulteren in versnelde cycli van celdeling.
Toepassingen van Embryonale Stamcellen
Embryonale stamcellen kunnen zich in vrijwel alle mogelijke celtypen ontwikkelen en zich in principe onbeperkt vernieuwen. Daarom worden ze onderzocht als mogelijke toepassing in de regeneratieve geneeskunde, bijvoorbeeld als mogelijke bron van donorweefsel.
ESC's zijn onder meer gebruikt bij aandoeningen als ruggenmergletsel, diabetes en neurodegeneratieve ziekten.
Stamcellen in Weefseltechnologie
In de weefseltechnologie is het gebruik van stamcellen van belang. Om een weefsel succesvol te kunnen ontwerpen, moeten de gebruikte cellen specifieke biologische functies kunnen uitvoeren, zoals de secretie van cytokines, signaalmoleculen, interactie met naburige cellen en het produceren van een extracellulaire matrix in de juiste organisatie.
Stamcellen vertonen deze specifieke biologische functies, samen met het vermogen om zichzelf te vernieuwen en te differentiëren in een of meer typen gespecialiseerde cellen. Embryonale stamcellen zijn een van de bronnen die worden overwogen voor het gebruik in de weefseltechnologie.
Ontwikkeling van Celtypen uit ESC's
Het gebruik van menselijke embryonale stamcellen heeft veel nieuwe mogelijkheden geopend voor de weefseltechnologie, maar er zijn nog veel horden die moeten worden genomen voordat menselijke embryonale stamcellen zelfs maar kunnen worden gebruikt. Onderzoek heeft zich gericht op het differentiëren van ESC's in verschillende celtypen voor uiteindelijk gebruik als celvervangende therapieën.
Enkele van de celtypen die zijn of momenteel worden ontwikkeld, zijn hartspiercellen, zenuwcellen, hepatocyten, beenmergcellen, eilandjes van Langerhanscellen en endotheelcellen. De vorming van dergelijke celtypen uit ESC's is echter niet zonder obstakels, daarom heeft het onderzoek zich gericht op het overwinnen van deze obstakels.
ESC's in Toxicologie en Medicijnontdekking
Er zijn studies gaande met ESC's om een alternatieve behandeling voor diabetes te bieden, met name door het programmeren van voorlopercellen. De ontwikkeling van een protocol voor de gerichte generatie van alvleeskliervoorlopercellen is uitgevoerd op hESC's (menselijke embryonale stamcellen).
Naast het feit dat ze een belangrijk alternatief zijn voor orgaantransplantaties, worden ESC's ook gebruikt op het gebied van toxicologie en als cellulaire screenings om nieuwe chemische stoffen te ontdekken die kunnen worden ontwikkeld als kleine-moleculaire geneesmiddelen. ESC-afgeleide hepatocyten zijn ook nuttige modellen die kunnen worden gebruikt in de preklinische stadia van onderzoek naar nieuwe geneesmiddelen.
De ontwikkeling van hepatocyten uit ESC's is echter moeilijk gebleken en dit belemmert het vermogen om het metabolisme van geneesmiddelen te testen.
Modellering van Genetische Aandoeningen met Stamcellen
Verschillende nieuwe studies zijn begonnen met het concept van het modelleren van genetische stoornissen met embryonale stamcellen. Ofwel door genetische manipulatie van de cellen, of meer recent, door het afleiden van zieke cellijnen die zijn geïdentificeerd door prenatale genetische diagnose (PGD), is het modelleren van genetische aandoeningen iets dat is bereikt met stamcellen.
Yury Verlinsky, een Russisch-Amerikaanse medisch onderzoeker die zich specialiseerde in embryo- en cellulaire genetica (genetische cytologie), ontwikkelde prenatale diagnostische testmethoden om op genen beruste en chromosomale aandoeningen anderhalve maand eerder te bepalen dan met een standaard vruchtwaterpunctie. De technieken worden nu gebruikt door veel zwangere vrouwen en toekomstige ouders, met name stellen met een voorgeschiedenis van genetische aandoeningen of waarbij de vrouw ouder is dan 35 (wanneer het risico op genetisch gerelateerde aandoeningen hoger is).
Savior Babies en HLA-Typing
Bovendien hebben ouders, door een embryo zonder genetische aandoeningen te selecteren, de mogelijkheid om het leven van broers en zussen te redden die al soortgelijke aandoeningen en ziekten hebben met behulp van cellen van het ziektevrije nageslacht. Dit wordt een savior baby, een donorbaby, een reddingsbaby of een baby op maat genoemd.
Hierbij wordt in-vitrofertilisatie gebruikt, waarbij de bevruchte eicel hetzelfde genetische humaan leukocytenantigeen (HLA-type) van een broertje of zusje met een bepaalde ziekte heeft. De bevruchte eicel is dus zelf vrij van de ziekte én heeft een kans om mesenchymatische stamcellen uit de navelstreng met stamceltransplantatie door te geven voor het genezen van de broer of zus, die lijdt aan een dodelijke ziekte, zoals kanker of anemie van Fanconi, die het beste behandeld kunnen worden met een hematopoëtische stamceltransplantatie.
Bevruchte eicellen worden getest op genetische compatibiliteit (typering van (HLA)), met behulp van pre-implantatiegenetische diagnostiek (PGD), en alleen bevruchte eicellen die compatibel zijn met het bestaande kind worden geïmplanteerd. Bevruchte eicellen worden ook getest om er zeker van te zijn dat ze vrij zijn van de oorspronkelijke genetische ziekte.
DNA-Schadeherstel in Stamcellen
Gedifferentieerde somatische cellen en embryonale stamcellen (ES-cellen) gebruiken verschillende strategieën om met DNA-schade om te gaan. Embryonale stamcellen (ES) gebruiken een andere strategie om met dubbelstrengsbreuken om te gaan.
Omdat ES-cellen ten grondslag liggen van alle celtypen van een organisme, inclusief de cellen van de kiembaan, zijn mutaties die ontstaan in ES-cellen als gevolg van gebrekkige DNA-reparatie een ernstiger probleem dan in gedifferentieerde somatische cellen. Bijgevolg zijn robuuste mechanismen nodig in ES-cellen om DNA-schade nauwkeurig te repareren, en als reparatie mislukt, om die cellen met niet-gerepareerde DNA-schade te verwijderen.
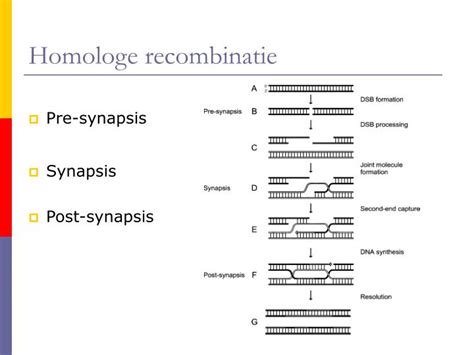
Homologe Recombinatie bij DNA-Reparatie
Zo gebruiken muizen-ES-cellen voornamelijk homologe recombinatiereparatie (HRR) om dubbelstrengsbreuken te repareren. Dit type reparatie is afhankelijk van de interactie van de twee zusterchromatiden die tijdens de S-fase worden gevormd en samen aanwezig zijn tijdens de G2-fase van de celcyclus. HRR kan dubbelstrengsbreuken in één zusterchromatide nauwkeurig repareren door intacte informatie van het andere zusterchromatide te gebruiken.
Cellen in de G1-fase van de celcyclus (d.w.z. na metafase/celdeling maar vóór de volgende ronde van replicatie) hebben slechts één kopie van elk chromosoom (d.w.z. zusterchromatiden zijn niet aanwezig).
Stamcellen in Moedermelk
In 2007 toonde professor Peter Hartmann en zijn team aan de University of Western Australia de aanwezigheid van stamcellen in moedermelk aan. Dr. Foteini Kakulas blijft nieuwe ontdekkingen doen, zoals de wetenschap dat deze op embryonale cellen gelijkende stamcellen in moedermelk kunnen worden aangestuurd om zich te ontwikkelen tot andere celtypen, zoals bot-, vet-, lever-, pancreas- en hersencellen.
Dit creëert nieuwe mogelijkheden om stamcellen te verkrijgen voor gebruik in de regeneratieve geneeskunde, zonder dat hiervoor embryo's moeten worden vernietigd. Dr. Kakulas presenteerde haar resultaten voor het eerst aan een Europees publiek tijdens een Medela Symposium. Ze verklaarde dat deze ontdekking het pad heeft geëffend voor onderzoek naar stamceltherapie en regeneratieve geneeskunde in het kader van bijvoorbeeld borstkankeronderzoek.
Migratie en Integratie van Moedermelkstamcellen
Onlangs nog presenteerde dr. Kakulas de laatste onderzoeksresultaten van haar celbiologieteam tijdens het 10e Symposium van Medela in Warschau. Hierin wordt de rol verklaard die deze cellen spelen in de ontwikkeling van baby's die borstvoeding krijgen. Baby's nemen dagelijks miljoenen, zelfs miljarden, levende cellen uit moedermelk in. Gebeurt dit toevallig? Kunnen deze cellen in de maag van de baby overleven?
Tijdens deze presentatie beschreef ze een recent experiment waarin ze bij muizen via een cross-fostering model naging wat er met deze cellen gebeurt. Met behulp van een markergen (TdTomato) bij muizen kon ze de weg volgen die de cellen afleggen vanaf de moedermelk tot in de pasgeborene. Bij deze experimenten zijn levende stamcellen van de moedermelk teruggevonden in de maag, maar ook in het bloed, de thymus, de lever, de pancreas, de milt en zelfs de hersenen. Deze cellen hadden zich ook functioneel geïntegreerd in deze organen en waren orgaanspecifieke eiwitten aan het produceren.
Deze resultaten zijn het eerste bewijs dat moedermelkstamcellen overleven bij pasgeborenen en wijzen erop dat deze cellen migreren en functioneel integreren in de organen van de pasgeborene, wat de ontwikkeling van de pasgeborene ten goede kan komen.
Dr. Kakulas zegt hierover: "Ik ben er trots op deel te kunnen nemen aan deze boeiende onderzoeken naar stamcellen in moedermelk, die door Medela worden gesteund. Ze hebben de deur geopend naar belangwekkend vervolgonderzoek. Aangezien stamcellen in relatief grote hoeveelheden aanwezig zijn in moedermelk, wil ik meer te weten komen over de rol die ze spelen op het vlak van weefselregeneratie en de ontwikkeling van de baby en over mogelijke effecten in het geval van ziekte."
Dr. Foteini Kakulas (voorheen Hassiotou) vervolgt: "Het is fantastisch om te zien hoe de biologie van stamcellen in moedermelk haar geheimen prijsgeeft en om nieuwe resultaten te demonstreren die onze kennis verdiepen. Dankzij de financiële steun van Medela kon ik dit onderzoek doen en op een andere manier aantonen waarom moedermelk zoveel meer betekent dan alleen voeding voor de baby. Bovendien wordt het duidelijk dat moedermelk kan dienen als ethisch verantwoorde, niet-invasieve en overvloedige bron van menselijke stamcellen. Er blijven echter tal van vragen onbeantwoord, voornamelijk over de functie van deze cellen voor de baby die borstvoeding krijgt. Ik ben er trots op dat ik deel kan nemen aan deze spannende ontdekkingsreis en ik zal dit onderzoek voortzetten aan de University of Western Australia."
Regeneron en Genetische Geneeskunde
Regeneron streeft naar innovatie en de ontdekking van levensveranderende medicijnen door open te staan voor meerdere benaderingen, bestaande technologieën te combineren en verbindingspunten te vinden op nieuwe en opwindende plaatsen. Genetische geneesmiddelen hebben tot doel genomen te worden om genomen te worden, waardoor genexpressie, silencing of editing mogelijk wordt.
Bij het nastreven van onderzoek naar genetische geneesmiddelen, worden er altijd verbindingen gelegd. Door gebruik te maken van een veelzijdige aanpak, worden bestaande toonaangevende technologieplatforms, zoals VelociSuite®, gebruikt en gecombineerd op nieuwe en opwindende manieren, wat betekent dat er niet alleen wordt gestopt bij het gebruik van antilichamen.
De toewijding aan het verkennen van meerdere strategieën maakt gebruik van de expertise van het bedrijf op het gebied van antilichamen, biologie, genetica en technologieontwikkeling, allemaal onder één dak, om nieuwe medicijnen te brengen aan mensen in nood. Genetische geneesmiddelen stellen Regeneron in staat om belangrijke doelwitten en programma's na te streven die verder gaan dan wat alleen met antilichamen kan worden bereikt.
Het bedrijf bevordert toonaangevende genetische geneeskunde technologieën door bestaande toonaangevende technologieplatforms toe te passen, zoals VelociSuite®. Genbewerking wordt gebruikt om genen te verstoren en conventionele gentherapie voor vervanging te heroverwegen. Externe samenwerkingen faciliteren de uitwisseling van kennis en innovatieve behandelingsbenaderingen, terwijl de expertise op het gebied van genetica en de fundering op het gebied van genomica de ruggengraat vormen van deze partnerschappen.
CRISPR en siRNA in de Medicijnontwikkeling
Regeneron was, samen met Intellia, de eerste die met succes CRISPR gebruikte voor transthyretin amyloidosis in een enkele dosis in een klinische proef. Regeneron loopt voorop in de ontdekking en ontwikkeling van siRNA-geneesmiddelen. Met een diepgaand begrip van menselijke biologie en genetica, is de rigoureuze, wetenschappelijk geleide aanpak van ontdekking klaar om de volgende golf van levensveranderende geneesmiddelen te informeren voor de meest moeilijk te behandelen ziekten.
Bij het nastreven van doorbraken in neurologische ziekten spelen genetische geneesmiddelen een cruciale rol bij het transformeren van het landschap van behandelingsopties. Cardiometabole stoornissen omvatten een breed spectrum van ziekten zoals hartfalen en leverziekten, en vormen een aanzienlijke uitdaging voor de gezondheidszorg. Genetische geneesmiddelen vormen een veelbelovende oplossing om dit diverse scala aan aandoeningen aan te pakken.
Patiëntgerichte Therapieën
De precisie-antilichaam-targetingtechnologie van Regeneron heeft de weg vrijgemaakt voor een nieuwe methode voor het leveren van vervangende enzymen. De succesvolle uitvinding van een reeks antilichamen die specifiek zijn ontworpen om enzymvervangende therapieën naar hun beoogde doelweefsel te leiden, biedt een veelbelovende behandelingsaanpak voor lysosomale stapelingsstoornissen.
Door ons te richten op plaatsen waar lokale toediening een optie is, zoals het binnenoor, kunnen nieuwe therapieën gemakkelijk worden beoordeeld zonder de complicaties van systemische toediening. De baanbrekende AAV-technologie van Regeneron en de kennis van het binnenoor maken snelle vooruitgang van therapeutische kandidaten mogelijk. Het doel is om interventies te creëren met behulp van siRNA-technologieën die een verminderde doseringsfrequentie mogelijk maken, waardoor de noodzaak van herhaalde toediening wordt geminimaliseerd.
Met ongeveer 1,7 miljard mensen wereldwijd getroffen door musculoskeletale aandoeningen en aanhoudende aanzienlijke onvervulde behoeften, valt gentherapie op als een cruciale oplossing, met name voor erfelijke ziekten zoals myasthenia gravis.
CRISPR uitgelegd
Navelstrengbloed en Stamceltransplantaties
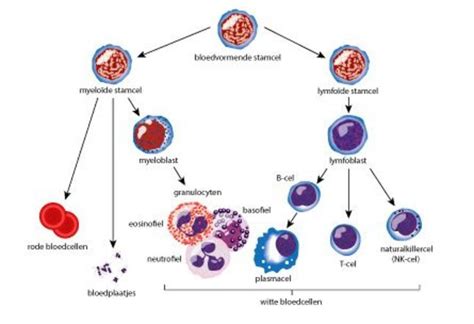
Navelstrengbloed is een belangrijke bron van stamcellen. Deze cellen zijn niet helemaal gelijk aan embryonale stamcellen omdat ze al wat verder gespecialiseerd zijn dan de embryonale stamcellen. Hoe dan ook bieden ze opties en worden ze onder andere gebruikt bij stamceltransplantaties bij mensen met bloedkanker.
Stamcellen uit navelstrengbloed zijn relatief makkelijk te verkrijgen. Bij de geboorte van een kind wordt de navelstreng doorgeknipt, op dat moment kan het navelstrengbloed in principe worden opgevangen. Het kan ook worden bewaard.
Geïnduceerde Pluripotente Stamcellen (iPS-cellen)
De ontdekking van ‘Induced Pluripotent Stem Cells’ (iPS-cellen) gebeurde in 2006, waarna de verantwoordelijke onderzoekers in 2012 de Nobelprijs voor geneeskunde kregen. IPS-cellen zijn afkomstig van huidcellen of bloedcellen die in het labo ‘geherprogrammeerd’ worden tot embryonale stamcellen en dus het vermogen terugkrijgen te differentiëren tot bijna alle lichaamscellen.
De cellen krijgen een cocktail van transcriptiefactoren, dit zet een complex proces in gang op celniveau en herstelt het pluripotente vermogen van de cellen. De gespecialiseerde cellen worden dus opnieuw stamcellen die alle richtingen uit kunnen. Deze doorbraak was enorm belangrijk voor het domein van de regeneratieve geneeskunde.
Voordelen en Uitdagingen van iPS-cellen
De ethische kwestie van de vernietiging van embryo’s valt weg. Het onderzoek naar deze cellen en hun mogelijkheden draait nog steeds op volle toeren. Dit onderzoek gaat voornamelijk uit naar hoe we de gevaren van het gebruik van iPS kunnen tegengaan.
Het risico op tumorvorming: stamcellen zijn aantrekkelijk door hun vermogen om oneindig veel te blijven delen. Het risico op afstoting door het immuunsysteem: dit kan een hevige shock veroorzaken en dodelijk zijn voor de patiënt. De mogelijkheid om iPS te maken van de patiënt zijn/haar eigen huidcellen geeft dus enorme voordelen om deze immuniteitsafstoting te vermijden; je lichaam herkent de getransplanteerde stamcellen immers als lichaamseigen en ziet er geen gevaar in.
Heterogeniteit: hiermee wordt bedoeld dat elke iPS-lijn verschillend is in morfologie, groeisnelheid, genexpressie en capaciteit om te differentiëren tot verschillende celtypes. Dit maakt het onderzoek naar en, uiteindelijk, de toepassingen voor stamceltherapieën een stuk ingewikkelder. Elke cellijn moet met de nodige, gepersonaliseerde, voorzichtigheid worden aangepakt.
Stamcelonderzoek in Nederland
Er worden steeds vaker stamcellen gebruikt voor onderzoek en experimentele therapieën, maar de klinische mogelijkheden van stamcellen zijn vooralsnog beperkt. Pluripotente stamcellen, met embryonale stamcellen als bekendste voorbeeld, kunnen differentiëren tot elk type cel; weefselspecifieke stamcellen daarentegen, kunnen nog slechts 1 of een aantal celtypen vormen binnen 1 type weefsel.
Sinds enige tijd is het mogelijk om verschillende typen somatische cellen te herprogrammeren tot pluripotente stamcellen. Dergelijke stamcellen worden geïnduceerde pluripotente stamcellen (iPS-cellen) genoemd. Ook uit cellen van patiënten met een genetische aandoening kunnen iPS-cellen gevormd worden. Daarmee kan tegen een specifieke genetische achtergrond, onderzoek gedaan worden naar ziektemechanismen en nieuwe medicijnen.
Klinische toepassing van dergelijke iPS-cellen is op korte termijn nog niet te verwachten. In verscheidene Nederlandse academische centra worden faciliteiten opgericht om iPS-cellen te maken voor wetenschappelijk onderzoek.