Hematopoëse, afgeleid van de Griekse woorden 'haîma' (bloed) en 'poieîn' (maken), is het proces waarbij bloedplaatjes en bloedcellen worden gevormd uit een multipotente, hematopoëtische stamcel. Dit anabole proces vindt voornamelijk plaats in het rode beenmerg en omvat de vorming van rode bloedcellen, bloedplaatjes en de vijf hoofdsoorten witte bloedcellen door middel van celdifferentiatie. Aangezien bloedcellen en bloedplaatjes een beperkte levensduur hebben, is voortdurende vernieuwing door nieuwe cellen vanuit de stamcellen in het beenmerg essentieel.
Hematopoëtische stamcellen (HSCs) zijn zelfvernieuwende, multipotente cellen die gedurende het hele leven alle bloedceltypes produceren. Zij zijn cruciaal voor het aanvullen van het beenmerg bij patiënten met bloedgerelateerde stoornissen. Een significante uitdaging in het stamcelonderzoek is het genereren van grote hoeveelheden van deze zeldzame cellen in vitro voor zowel onderzoek als klinisch gebruik. Dit is momenteel uiterst moeilijk, aangezien nog niet alle stappen die leiden tot de generatie van HSC's in vivo volledig zijn opgehelderd.
Het algemene doel van het onderzoek is het verhelderen van de cellulaire en moleculaire gebeurtenissen die leiden tot de productie en expansie van HSC's tijdens de embryonale ontwikkeling. Alle HSC's worden gevormd tijdens de embryonale ontwikkeling uit gespecialiseerde endotheelcellen met een hemogeen potentieel. Deze hemogene endotheelcellen zijn aanwezig in de aorta, waar ze intra-aortische hematopoëtische clusters (IAHC's) vormen. Deze clusters bevatten echter slechts een klein aantal HSC's, waardoor de identiteit van de meeste IAHC-cellen onbekend blijft. Het onderzoek richt zich op het blootleggen van de essentiële factoren die de embryonale HSC-productie reguleren.
Ontwikkeling van Hematopoëse tijdens de Embryonale Periode
Op embryonale dag (E) 10,5 maken HSC's deel uit van intra-aortische hematopoëtische clusters (IAHC's) die nauw verbonden zijn met het endotheel van de aorta. Nieuwe experimentele beeldvormingstechnieken maken het mogelijk de dynamische vorming van HSC's direct in de aorta van het muizenembryo te observeren. Tijdens de endotheel-naar-hematopoëtische overgang (EHT) worden sterke celbewegingen en modificaties aan het oppervlaktemembraan waargenomen, wat wijst op belangrijke rollen voor celadhesiemoleculen en de herschikking van het microtubulus (MT) cytoskelet. Het onderzoek wil de basisbiomechanica van embryonale HSC-formatie begrijpen, met een focus op MT-regulerende eiwitten die betrokken zijn bij celpolariteit, asymmetrische celdeling, adhesie en migratie.
Het ontstaan van HSC's vindt voornamelijk plaats in het ventrale aspect van de embryo-aorta (waargenomen bij zebravissen, kippen, muizen en mensen). Dit proces wordt strikt gereguleerd in tijd en ruimte door signalen die de omringende micro-omgeving uitzendt. De precieze lokalisatie van HSC-opkomst in de aorta van deze soorten maakt ze tot krachtige modellen om moleculaire signalen uit omringende weefsels te bestuderen en hematopoëtische activiteit te beperken tot specifieke gebieden. Moderne technologieën worden ingezet om genen te ontcijferen die differentiële expressie vertonen in specifieke regio's van de aorta tijdens HSC-generatie.
Bij zoogdieren blijft de anatomische locatie van de oorsprong van HSC's controversieel, deels omdat het bloed al circuleert wanneer HSC's detecteerbaar zijn, wat celuitwisseling tussen weefsels kan veroorzaken. Na elf weken zwangerschap kan een embryo zijn voedingsstoffen via het bloed van de moeder verkrijgen. In de eerste weken van de ontwikkeling krijgt het embryo zijn voeding echter op een andere manier. Kliercellen in de baarmoederwand slaan glucose op in de vorm van glycogeen, dat vervolgens samen met glycoproteïnen aan de placenta wordt geleverd. Deze voedingsstoffen voorzien het embryo van energie en worden omgezet in aminozuren, de bouwstenen voor verdere groei. Na elf weken, wanneer een connectie tussen de bloedsomloop van de moeder en de placenta tot stand is gekomen, worden deze kliercellen minder actief.
Deze ontdekking biedt een belangrijke vooruitgang in het begrip van nutriëntentransport van de moeder naar het kind in de baarmoeder. Het onderzoek benadrukt ook het belang van een gezonde voeding tijdens de eerste elf weken van de zwangerschap, en zelfs al vóór de zwangerschap, aangezien voedingsstoffen al vóór de conceptie in de kliercellen worden opgeslagen. De resultaten verduidelijken ook eerdere bevindingen, zoals de verhoogde vatbaarheid voor bepaalde gezondheidsproblemen bij kinderen van moeders die tijdens de hongersnood aan het einde van de Tweede Wereldoorlog minder dan drie maanden zwanger waren.
Hematopoëse bij de Mens: Vroege Ontwikkeling
De menselijke hematopoëse initieert zich in de dooierzak tijdens de derde week van de ontwikkeling. Tegelijkertijd ontstaat ook de capaciteit om bloedcellen te produceren in het embryo, binnen de splanchnopleura. Dit potentieel wordt echter pas tot expressie gebracht na dag 27, wanneer geclusterde hematopoëtische stamcellen uit de ventrale wand van de aorta en de vitelline arterie verschijnen. De uitstulping van hematopoëtische cellen vanuit vaatwanden weerspiegelt de herdifferentiatie van lokale endotheelcellen, die waarschijnlijk afkomstig zijn van angio-hematopoëtische mesodermale voorlopers die uit de splanchnopleura zijn geëmigreerd.
De stamcellen die afkomstig zijn uit de dooierzak zijn beperkt tot myelo-erythroïde ontwikkeling. De stamcellen die in het embryo ontstaan, zijn daarentegen ook lymfopoëtisch. Zij vertegenwoordigen de eerste multipotente, volwassen bloedvoorlopers die verschijnen in de menselijke ontogenie, kort voor het begin van de leverhematopoëse. Deze bevindingen hebben geleid tot de vaststelling van een nieuwe hiërarchie van bloedvormende weefsels in de menselijke ontwikkeling en een heroverweging van de oorsprong van definitieve menselijke hematopoëse.
Hematopoiesis - Vorming van bloedcellen, animatie
Fases van Embryonale Hematopoëse
De bloedcelontwikkeling begint reeds op de 7e dag van het embryonale leven. Rode bloedcellen (RBC's) spelen een cruciale rol bij de zuurstoftoevoer en de vorming van vasculaire kanalen tijdens de embryogenese. De hematopoëtische ontogenie omvat twee belangrijke ontwikkelingsfasen: de initiële productie van primitieve erytroïde cellen (EryP), gevolgd door de opkomst en expansie van definitieve erytroïde cellen (EryD), die vervolgens de overhand krijgen. Een volledig falen van de primitieve erytropoëse is embryonaal letaal.
Het begrijpen van embryonale hematopoëse biedt essentiële inzichten in de oorsprong van congenitale anemieën en hematologische stoornissen. Vroege identificatie van verstoringen in de erytroïde lijnontwikkeling kan leiden tot tijdige diagnostische en therapeutische interventies, met name bij zwangerschappen met een hoog risico. Clinici die deze ontwikkelingsprocessen begrijpen, zijn beter uitgerust om neonatale hematologische abnormaliteiten te interpreteren en langetermijncomplicaties te anticiperen.
Gastrulatie en de Vroege Golf van Hematopoëse
De gastrulatie begint met de epiblast, een enkele epitheliale cellaag, die zich differentieert in de drie embryonale kiemlagen: ectoderm, mesoderm en endoderm. Binnen de eerste twee weken van de dracht wordt de initiële golf van primitieve hematopoëtische en endotheelcelontwikkeling getriggerd door signalering naar de extra-embryonaire, endodermale dooierzak. Deze golf resulteert voornamelijk in de vorming van EryP-cellen, megakaryocyten, macrofagen en endotheelcellen.
EryP-cellen zijn groter dan hun voorlopers, behouden hun kern, drukken embryonale globines uit en zijn beperkt tot de dooierzak. Deze cellen dragen bij aan de vorming van bloedeilanden - structuren waarin centraal gelegen cellen differentiëren tot erytroïde en myeloïde lijnen, terwijl perifere cellen endotheelcellen worden die zich organiseren tot vasculaire kanalen. Deze bloedeilanden versmelten uiteindelijk tot een onderling verbonden vasculair netwerk dat de dooierzak bestrijkt.
Oscillerende Bloedstromen en de Transitie naar Definitieve Hematopoëse
Oscillerende plasmafluxen, aangedreven door het zich ontwikkelende hart, transporteren EryP en andere primitieve cellen door deze vasculaire kanalen. Eenmaal in de circulatie ondergaan EryP-cellen enucleatie in de foetale lever, waarna macrofagen de geëxtrudeerde kernen opruimen. De productie van EryP is van voorbijgaande aard en vindt alleen plaats tijdens de vroege fase van de vascularisatie van de dooierzak. De resterende voorlopercellen blijven echter rijpen, evolueren van pro-erythroblast naar orthochromatische erythroblast tot reticulocyt, en blijven tot minstens de geboorte in de bloedbaan aanwezig.
Kort na de ontwikkeling van EryP ontstaan hoog-proliferatieve, multipotente voorlopers (MPP's) in de dooierzak. Deze cellen initiëren de eerste golf van definitieve hematopoëse en geven aanleiding tot EryD. Soms aangeduid als erytroïde/myeloïde voorlopers, dienen deze cellen als een overgangspopulatie tussen primitieve erytropoëse en hematopoëse afkomstig van hematopoëtische stamcellen (HSC's). Deze voorlopers migreren naar en koloniseren de foetale lever, de volgende definitieve hematopoëtische plaats tijdens de dracht.
De Rol van de Aorta in HSC Generatie
De tweede golf van definitieve hematopoëse vervangt zowel de primitieve hematopoëse als de eerste golf van definitieve hematopoëse. HSC's ontstaan uit hemogeen endotheel, gelegen in de ventrale wand van de zich ontwikkelende aorta, specifiek in een regio die bekend staat als de para-aortische splanchnopleura. Deze structuur geeft aanleiding tot de aorta-gonad-mesonephros (AGM)-regio, die de primaire intra-embryonaire plaats voor HSC-generatie is.
Tegen de zevende week van de dracht migreren HSC's naar en koloniseren de foetale lever, waar ze prolifereren en beginnen te differentiëren. In dit stadium wordt de lever de dominante plaats van hematopoëse. HSC's koloniseren ook tijdelijk de milt rond de 20e week en dragen gedurende een korte periode bij aan de erytropoëse. Gelijktijdig beginnen HSC's het beenmerg te bezetten - een cruciale transitie, aangezien het beenmerg uiteindelijk de primaire plaats van erytropoëse wordt naarmate de dracht vordert.
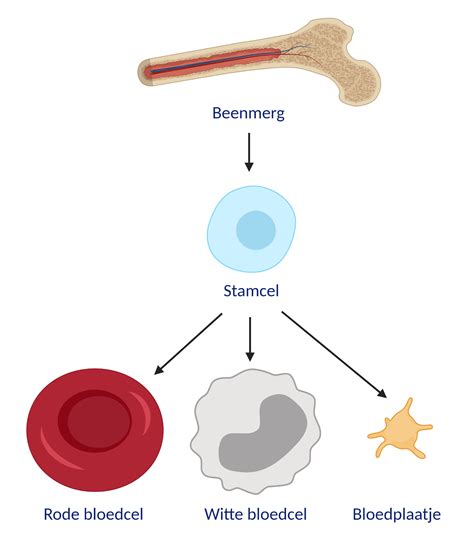
Vorming van Bloedcellen en Hun Functies
Hematopoëse is het proces waarbij het lichaam nieuwe bloedcellen produceert. Bij volwassenen vindt hematopoëse voornamelijk plaats in het beenmerg. In de vroege ontwikkeling, zoals tijdens de groei van de foetus, kan hematopoëse ook in andere organen plaatsvinden, zoals de lever en de milt.
Verschillende Typen Bloedcellen
De belangrijkste soorten bloedcellen die worden geproduceerd door hematopoëse zijn:
- Rode bloedcellen (erytrocyten): Deze cellen zijn verantwoordelijk voor het transport van zuurstof door het lichaam.
- Witte bloedcellen (leukocyten): Deze cellen maken deel uit van het immuunsysteem en helpen het lichaam infecties te bestrijden.
- Bloedplaatjes (trombocyten): Deze celfragmenten zijn essentieel voor de bloedstolling.
Ontwikkelingsproces van Stamcellen
Het ontwikkelingsproces van een stamcel in het beenmerg verloopt onder invloed van groeifactoren. Naarmate het ontwikkelingsproces vordert, wordt het eindresultaat sterker vastgelegd en zijn de differentiatiemogelijkheden beperkter. De vorming van bloed met alle differentiaties omvat een reeks voorlopercellen:
- Hematopoëtische stamcel
- Myeloïde voorlopercel
- Lymfoïde voorlopercel
- Granulocyt/monocytvoorlopercel
- Eosinofiele voorlopercel
- Basofiele voorlopercel
- Megakaryocyt
- Erytroïde voorlopercel
- T-voorlopercel
- B-voorlopercel
- Dendritische cel
- Monocyt
- Neutrofiel
- Eosinofiel
- Basofiel
- Bloedplaatjes of trombocyten
- Rode bloedcel of erytrocyt
- Macrofagen
- Natural killer-cel
- T-helper-cel
- Cytotoxische T-cel
- B-cel
Klinische Significatie en Aandoeningen
Bij de ziekte leukemie is de hematopoëse ernstig verstoord. In zeldzame gevallen kan er een onvermogen ontstaan van de beenmergcellen om uit te rijpen, waardoor het lichaam steeds minder bloedcellen, of steeds minder bloedcellen van een bepaalde soort aanmaakt. Dit kan leiden tot een reeks symptomen, afhankelijk van het type bloedcel dat is aangetast.
Bloedarmoede en Hemoglobineproductie
Bloedarmoede treedt op wanneer er een tekort is aan rode bloedcellen of hemoglobine, wat leidt tot vermoeidheid en zwakte. Een verstoorde ontwikkeling van hemoglobine A (HbA) kan aanzienlijke gevolgen hebben voor pasgeboren kinderen tot in de volwassenheid.
Bèta-thalassemie is een genetische mutatie waarbij de synthese van de bèta-globineketen verminderd of afwezig is. Beperkte bèta-globineproductie vermindert de hemoglobine- en RBC-aanmaak, wat bloedarmoede veroorzaakt. Meer dan 200 mutaties zijn gemeld, waarvan de meeste voortkomen uit puntmutaties in functioneel essentiële genregio's voor bèta-globineketenproductie. Een verminderd aanbod van bèta-globineketens leidt tot een overschot aan alfa-globineketens, die zich ophopen en aggregeren in het beenmerg. De conglomeratie van alfa-globineketens leidt tot vroegtijdige celdood van erytroïde voorlopers en ineffectieve erytropoëse. Bloedarmoede stimuleert de productie van erytropoëtine (EPO), en deze drang om meer RBC's te produceren resulteert in extramedullaire hematopoëse.
Sikkelcelanemie is het gevolg van een niet-conservatieve missense-mutatie, waarbij een enkele nucleotideverandering optreedt in het bèta-globinegengebied. Deze mutatie zorgt ervoor dat RBC's een "sikkelvorm" aannemen wanneer ze gedeoxygeneerd zijn. Deze gesikkelde RBC's, die hemoglobine S (HbS) bevatten, kunnen voortdurend van vorm veranderen, wat leidt tot hun vroegtijdige vernietiging intravasculair. In hun gesikkelde vorm hebben de RBC's de neiging zich vast te zetten in de haarvaten, wat leidt tot vaso-occlusie. Overmatige vaso-occlusie kan resulteren in een sikkelcel-pijnaanval.
In beide ziekten heeft hydroxyureum de kwaliteit van leven van patiënten verbeterd. Dit medicijn verhoogt de niveaus van foetaal hemoglobine (HbF) in de bloedbaan. Aangezien HbF geen bèta-globineketens bevat, wordt het niet beïnvloed door de mutaties die deze ziekten veroorzaken.
tags: #hematopoiese #in #foetus #ontwikkeling