Innovatieve Brandwondenbehandeling met Gekweekte Huid
In het Brandwondencentrum van het Maasstad Ziekenhuis is voor het eerst in Nederland een baby met ernstige brandwonden behandeld met gekweekte huid afkomstig van de baby zelf. Van de baby was zeventig procent van het lichaamsoppervlak verbrand. In een laboratorium werden kleine gezonde stukjes huid van de baby gebruikt om nieuwe huidcellen te kweken. Vervolgens kon de gekweekte huid op de brandwond worden teruggeplaatst.
De baby was de jongste patiënt ooit die de DenovoSkin-behandeling heeft ondergaan, buiten een onderzoekssetting. De behandeling is een innovatieve techniek waarbij een klein stukje gezonde huid van de patiënt wordt gebruikt om in het laboratorium nieuwe huidcellen te kweken. Deze gekweekte huid wordt teruggeplaatst op de wond. Omdat het om het eigen weefsel van de patiënt gaat, is de kans op afstoting minimaal.
DenovoSkin werkt anders dan de behandelingen die tot nu toe worden toegepast. Bij reguliere behandelingen wordt huid uit gezonde delen gehaald van bijvoorbeeld de rug of de dijen. Maar wanneer de lederhuid ontbreekt, is de kans heel groot dat er littekenweefsel ontstaat. Dat zorgt voor grote, pijnlijke littekens die de bewegingsvrijheid van patiënten kunnen beperken. Bovendien is er bij grote brandwonden soms niet genoeg gezonde huid beschikbaar om de brandwonden te bedekken.
Trauma- en brandwondenchirurg in het Brandwondencentrum van het Maasstad Ziekenhuis, Kees van der Vlies, vertelt dat de baby succesvol is geopereerd en goed herstelt. “Wij zijn trots dat we deze behandeling hebben kunnen toepassen. Het maakt echt een verschil voor patiënten met ernstige, grote/uitgebreide brandwonden en draagt bij aan een betere levenskwaliteit.” De DenovoSkin-behandeling werd klinisch getest door het Brandwondencentrum van het Maasstad Ziekenhuis samen met het Zwitserse biotechbedrijf CUTISS AG, dat de techniek heeft ontwikkeld, en onderzoekscentrum Wyss Zurich.
Stamcellen: Definitie en Types
Stamcellen zijn cellen uit het lichaam die kunnen veranderen in een ander celtype van het lichaam. Dit wordt differentiatie genoemd. Deze cellen kunnen onbeperkt delen en produceren rijpe dochtercellen. Ze zijn dus bouwstenen van verschillende weefsels en organen.
Totipotente Stamcellen
Totipotente stamcellen kunnen als enkele cel een nieuw individu vormen. Een voorbeeld hiervan is de zygote, waarbij een zaadcel versmelt met een eicel. De cel zal zich nog een aantal keer delen in de eerste uren na de bevruchting, waardoor meerdere totipotente cellen ontstaan. Wanneer we zo’n totipotente cel zouden terugplaatsen in de baarmoeder, zou deze uitgroeien tot een foetus. Zo ontstaan eeneiige tweelingen.
Pluripotente Stamcellen
Na ongeveer 4 à 5 dagen na de bevruchting ontstaat er een type cel die de blastocyste wordt genoemd. Deze cel bestaat uit een holte met aan de buitenkant een laag cellen die zich ontwikkelt tot de placenta. Pluripotente stamcellen kunnen veranderen in alle drie kiemlagen van het embryo in de blastocyste. Deze kiembladen zijn het ectoderm, het mesoderm en het endoderm.
- Het ectoderm zal het centrale zenuwstelsel vormen, maar ook de zenuwcellen, de haren, de tanden, de sensorische cellen van de ogen, de oren, de neus, de mond en de pigmentcellen.
- Het mesoderm zorgt voor het ontstaan van de spieren, het bloed, de bloedvaten, het bindweefsel en het hart.
- Het endoderm zal in staat zijn om het maagdarmstelsel, de longen, de blaas en de kiemcellen te vormen.
Het extra-embryonaal weefsel zal niet meer kunnen worden gecreëerd door de pluripotente stamcellen.
Multipotente Stamcellen
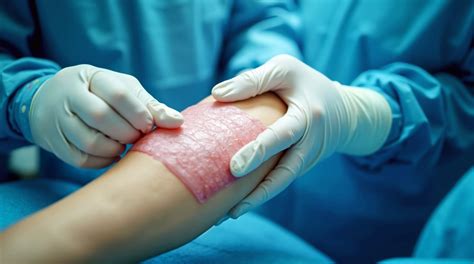
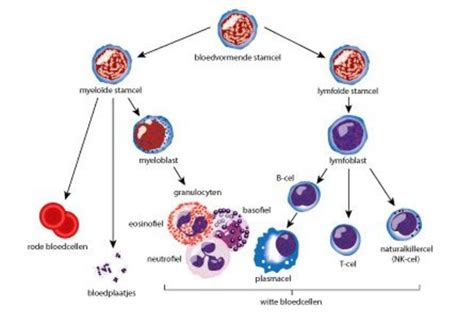
Multipotente stamcellen kunnen in een beperkt aantal cellen differentiëren. Ze kunnen veranderen in meerdere celtypes van een bepaald weefsel. Hun functie houdt in om bepaalde cellen met een korte levensduur te verversen. Een voorbeeld van zo’n multipotent stamceltype is de hematopoëtische stamcel die te vinden is in het beenmerg. Uit deze stamcellen worden bloedcellen (rode bloedcellen, witte bloedcellen en bloedplaatjes) ontwikkeld. De bloedcellen hebben een beperkte levensduur en moeten voortdurend worden vervangen. De multipotente stamcellen zijn dus niet enkel belangrijk bij de vroege ontwikkeling, maar spelen ook bij kinderen en volwassenen een grote rol.
Bronnen van Stamcellen
Embryonale Stamcellen
Stamcellen kunnen uit verschillende weefsels geïsoleerd worden. Zo kunnen stamcellen in de binnenste laag van de blastocysten in kweek worden gebracht. Deze embryonale stamcellen zijn pluripotent en worden gehaald uit restembryo’s uit IVF (In-vitrofertilisatie). Bij IVF wordt er één embryo ingeplant bij de vrouw en de rest kan worden gebruikt voor stamcelonderzoek, mits de ouders hier toestemming voor geven.
Het embryo zal uiteindelijk uitgroeien tot een foetus waarbij er meer multipotente stamcellen aanwezig zijn dan bij een pasgeboren baby. Deze foetale stamcellen worden vooral verkregen bij een abortus. Omwille van ethische problemen zal deze manier om stamcellen te isoleren minder vaak gebruikt worden.
Navelstrengbloed
De navelstreng is een bron van stamcellen. Deze wordt na de geboorte meestal weggegooid, waardoor deze manier ethisch verantwoord is. De stamcellen die zich in de navelstreng bevinden zijn relatief makkelijk te isoleren en bovendien op een pijnloze manier. Navelstrengbloed is een belangrijke bron van stamcellen. Deze cellen zijn niet helemaal gelijk aan embryonale stamcellen omdat ze al wat verder gespecialiseerd zijn. Hoe dan ook bieden ze opties en worden ze onder andere gebruikt bij stamceltransplantaties bij mensen met bloedkanker. Stamcellen uit navelstrengbloed zijn relatief makkelijk te verkrijgen. Bij de geboorte van een kind wordt de navelstreng doorgeknipt; op dat moment kan het navelstrengbloed in principe worden opgevangen en bewaard.
Volwassen Stamcellen
Organen in het lichaam bezitten ook een kleine hoeveelheid stamcellen. Wanneer een orgaan aangetast wordt, zullen de stamcellen in dat orgaan de aangetaste cellen vervangen. Deze stamcellen zijn multipotent en kunnen verder ook aanwezig zijn in het hart, de huid, de bloedvaten en de tanden. Volwassen stamcellen zijn overal in het lichaam te vinden. Zo vind je in de lever leverstamcellen en in de huid huidstamcellen. Deze volwassen stamcellen zijn relatief makkelijk te verkrijgen, namelijk met een bloedafname. Dit doet geen pijn en is niet invasief. Volwassen stamcellen worden vandaag gebruikt voor de behandelingen van bloedziekten.
Mesenchymale stamcellen (MSC's) vormen veelbelovende stamcelbronnen voor het herstel/de regeneratie van beschadigde weefsels/organen. Naast hun toepassing voor het herstellen van beschadigde weefsels, zijn MSC's ook gebruikt voor de behandeling van auto-immuunziekten en GVHD (graft-versus-hostreactie) vanwege hun immuunregulerende eigenschappen. Veel klinische onderzoeken hebben aangetoond dat MSC's de genezing van verschillende wonden kunnen bevorderen, waaronder chronische huidzweren veroorzaakt door diabetes mellitus, blootstelling aan straling en ischemie. Ook zijn de voordelen van MSC's in een hypertrofisch littekenmodel van konijnenoren gerapporteerd. Gezien de immuunregulerende eigenschappen van MSC's is het goed mogelijk dat MSC's littekenloze wondgenezing bevorderen.
Toepassingen van Stamceltherapie
Beenmergtransplantatie
Er bestaan veel toepassingen van stamcellen. Ze worden vooral toegediend wanneer een patiënt lijdt aan een ziekte waarbij cellen afsterven of slecht functioneren. Patiënten met leukemie kunnen een beenmergtransplantatie ondergaan. Ze krijgen chemo- en radiotherapie om de kwaadaardige witte bloedcellen te vernietigen. Hierbij sterven ook een aantal gezonde bloedcellen af. De patiënt kan geholpen worden door het krijgen van bloedstamcellen zodat er weer een nieuwe populatie gezonde cellen ontstaat. Hiervoor zal men eerst wat beenmerg moeten wegnemen van de patiënt. Dit is echter een pijnlijke ingreep. Sommige leukemiepatiënten beschikken over onvoldoende bloedstamcellen in het beenmerg, waardoor ze een beenmergdonor nodig hebben.
Hartziekten
Een andere toepassing van stamceltherapie wordt gebruikt bij het krijgen van een hartinfarct. Een hartinfarct zorgt voor een vermindering van de hartspiercellen doordat de cellen geen zuurstof meer krijgen. De hartspiercellen die overblijven zullen bijgevolg een hardere pompfunctie uitvoeren. Stamcellen kunnen gebruikt worden om de afgestorven hartspiercellen te vervangen door nieuw gezond hartspierweefsel. Deze ingreep is helaas niet zo eenvoudig. Men gaat vaak eerder een harttransplantatie overwegen dan een therapie met stamcellen.
Eerste experimenten met betrekking tot stamceltherapie wijzen in positieve richting wat de slaagkansen van deze nieuwe vorm van therapie betreft. Zo ziet men reeds een herstel van chronisch ischemisch myocardweefsel na myocardinfarct nadat men circa 25,5 × 106 ongedifferentieerde mononucleaire beenmergstamcellen transendocardiaal autotransplanteerde op de plaatsen waar zich hibernerende myocardcellen bevonden. En hoewel uit onderzoek reeds is gebleken dat pluripotente stamcellen in staat zijn zich te differentiëren tot cardiomyocyten en endotheliale cellen, lijkt het er in dit experiment echter op dat het injecteren van de mononucleaire beenmergstamcellen eerder heeft bijgedragen tot de angio(neo)genese (vorming van nieuwe bloedvaten). Beenmergcelcomponenten secerneren immers een gamma aan cytokines, fibroblast groeifactoren en vasculaire endotheliale groeifactoren die allen bijdragen tot het natuurlijke proces van angiogenese.
Toch moet er nog steeds voorzichtig worden omgesprongen met deze resultaten. Niet alle resultaten uit dierproeven zijn zonder meer te vertalen naar toepassingen op de mens, tevens tonen niet alle studies een immer positief beeld. Zo kan het gebeuren dat toediening van groeifactoren geen effect teweegbrengt of dat tumorvorming gestimuleerd wordt.
Neurologische Aandoeningen
Verder is stamceltherapie nuttig bij ziektes die de hersenen aantasten zoals de ziekte van Parkinson. Hiervoor moet verder wetenschappelijk onderzoek gedaan worden.
Beenmergfibrose
In het beenmerg komt de vorming van bloedcellen letterlijk in de verdrukking. Wetenschappers van het Erasmus MC zijn een stapje dichter bij de ontrafeling van het ziekteproces. “Bloedvormende cellen in het beenmerg die geleidelijk worden verdrongen door dikke vezels en littekenweefsel,” zo karakteriseert dr. Rebekka Schneider de aandoening waar zij onderzoek naar verricht. “De wetenschappelijke naam is beenmergfibrose. Er zijn verschillende ziekten bekend waarbij dit proces plaatsvindt, de bekendste is myelofibrose. Beenmergfibrose ontstaat als bloedvormende stamcellen gaan woekeren in het beenmerg. Er treedt dan fibrose op: de vorming van littekenweefsel. Dat proces verloopt zo heftig, dat de productie van bloedcellen in het gedrang komt.” Schneider: “Een deel van de cellen in het beenmerg bevat Gli1, een eiwit dat een rol speelt in de ontwikkeling van het embryo tot volwassene, de rijping van cellen, maar ook in het ontstaan van kanker. De onderzoekers toonden aan dat het Gli1-eiwit een cruciale rol speelt: “Als we de Gli1-bevattende cellen remmen, wordt beenmergfibrose voorkomen en blijft het beenmerg actief nieuwe bloedcellen vormen.” Schneider verwacht dat het remmen van de Gli1-cellen een veelbelovende therapie kan worden: “De huidige behandeling van myelofibrose bestaat uit transplantatie met stamcellen van een donor, maar bij veel patiënten slaat die behandeling niet goed aan.”
Technieken en Uitdagingen in Stamcelonderzoek
Cultiveren van Stamcellen
Het onderzoek naar stamceltherapie staat nog in zijn beginfase, met name bij het trachten opzetten van humane stamcellijnen. Het oogsten lukt reeds, het cultiveren en prolifereren lukt slechts in enkele centra ter wereld. De Zuid-Koreaanse overheid stimuleert al geruime tijd stamcelonderzoek en reproductief klonen; baanbrekend zijn de resultaten van Dr. Hwang Woo Suk en zijn team. In december 2005 is echter ontdekt dat de spectaculaire resultaten van Dr. Hwang Woo Suk volledig bleken te zijn gefabriceerd. Naar aanleiding van dit fraudeschandaal werden hij en zes andere leden van zijn team op 9 februari 2006 door de universiteit geschorst.
In China pasten rond 2005 Dr. Huang Hongyun en zijn team stamceltherapie toe op ALS-patiënten en andere neurologische patiënten, zoals mensen met een dwarslaesie. De cellen werden geoogst uit de reukzenuw van geaborteerde foetussen en werden in het hersenvocht gespoten.
Cultiveren (telen of verveelvoudigen) van cellen doet men door deze cellen op een speciale voedingsbodem, feeder-layers, te enten (aan te brengen) en door deze onder de juiste omstandigheden te brengen, gaan de cellen zich vermenigvuldigen. Het is de bedoeling dat er geen spontane niet-gecontroleerde differentiaties van deze cellen optreden, dus dat ze ongedifferentieerd blijven tijdens het cultiveringsproces. Embryonale muizenstamcellen kunnen vrij gemakkelijk ongedifferentieerd in kweek worden gehouden door het toevoegen van LIF (leukemia inhibite factor). De problemen die men moet trotseren bij het werken met humane embryonale stamcellen zijn onder andere het vinden van het juiste voedingsmilieu voor deze cellen, het vermijden van contaminatie van de cellijnen door deze voedingsbodems (bijvoorbeeld muizenbindweefsel feederlayer), het afstellen van de juiste groei- en andere factoren voor het aanzetten tot prolifereren (vermenigvuldigen) van de cellen en het correct "enten" van deze proliferaties op nieuwe bodems.
Recentelijk zijn er in het Utrechtse Hubrecht laboratorium enkele Nederlandse lijnen geïsoleerd. Na het cultiveren van humane stamcellijnen kan men overgaan tot het differentiëren van deze stamcellen naar cellen, weefsels of organen met de gewenste histologie.
Ethiek en Regelgeving
In de Verenigde Staten zijn federale subsidies voor onderzoek met gebruik van embryo’s verboden sinds 1995. Het onderzoek blijft onderwerp van publieke debatten. Voorstander van onderzoek met embryo’s is voormalig first lady Nancy Reagan. Haar echtgenoot Ronald Reagan leed aan de ziekte van Alzheimer, die genezen zou kunnen worden met stamceltherapie.
In België is stamcelonderzoek met embryonale stamcellen toegestaan onder strikte wettelijke voorwaarden. De cellen moeten bijvoorbeeld worden opgepikt voor dag 12 van de celdeling. Het is verboden zomaar eender wie eender wat te laten onderzoeken. Momenteel staat het onderzoek op embryonale stamcellen nog in zijn kinderschoenen en krijgt het te maken met ethische bezwaren en politieke tegenwind. Het heikele punt is dat het oppikken van embryonale stamcellen het embryo zelf vernietigt. Toepassingen van embryonale stamcellen in medische therapieën lijken dus - op dit moment - nog niet echt aan de orde. Al zijn onderzoekers positief over de mogelijkheden die embryonale stamceltherapieën kunnen bieden.
Per 1 januari 2007 wordt klinische stamceltherapie in Nederland verboden. Volgens het ministerie van Volksgezondheid zijn er nog te veel risico’s aan stamceltherapie verbonden.
Induced Pluripotent Stem Cells (iPS-cellen)
De ontdekking van ‘Induced Pluripotent Stem Cells (iPS-cellen)’ gebeurde in 2006, waarna de verantwoordelijke onderzoekers in 2012 de Nobelprijs voor geneeskunde kregen. iPS-cellen zijn afkomstig van huidcellen of bloedcellen die in het labo ‘geherprogrammeerd’ worden tot embryonale stamcellen en dus het vermogen terugkrijgen te differentiëren tot bijna alle lichaamscellen. De cellen krijgen een cocktail van transcriptiefactoren, dit zet een complex proces in gang op celniveau en herstelt het pluripotente vermogen van de cellen. De gespecialiseerde cellen worden dus opnieuw stamcellen die alle richtingen uit kunnen. Deze doorbraak was enorm belangrijk voor het domein van de regeneratieve geneeskunde. De ethische kwestie van de vernietiging van embryo’s valt weg. Het onderzoek naar deze cellen en hun mogelijkheden draait nog steeds op volle toeren. Dit onderzoek gaat voornamelijk uit naar hoe we de gevaren van het gebruik van iPS kunnen tegengaan.
Het risico op tumorvorming: stamcellen zijn aantrekkelijk door hun vermogen om oneindig veel te blijven delen. Het risico op afstoting door het immuunsysteem: dit kan een hevige shock veroorzaken en dodelijk zijn voor de patiënt. De mogelijkheid om iPS te maken van de patiënt zijn/haar eigen huidcellen geeft dus enorme voordelen om deze immuniteitsafstoting te vermijden; je lichaam herkent de getransplanteerde stamcellen immers als lichaamseigen en ziet er geen gevaar in. Heterogeniteit: hiermee wordt bedoeld dat elke iPS-lijn verschillend is in morfologie, groeisnelheid, genexpressie en capaciteit om te differentiëren tot verschillende celtypes. Dit maakt het onderzoek naar en, uiteindelijk, de toepassingen voor stamceltherapieën een stuk ingewikkelder. Elke cellijn moet met de nodige, gepersonaliseerde, voorzichtigheid worden aangepakt.
Wat zijn stamcellen? - Craig A. Kohn
Stamcelonderzoek en Toekomstige Perspectieven
Wetenschappers van het LUMC onderzoeken of de kans op afstoting wordt verkleind wanneer er lichaamseigen materiaal wordt gebruikt bij de behandeling van patiënten met een nieuwe donornier, door geherprogrammeerde stamcellen toe te dienen. Tijdens het onderzoek wordt in eerste instantie de veiligheid van de therapie getest. In een later stadium wordt gekeken of de behandeling ook voorkomt dat de donornier wordt afgestoten.
Recent is men begonnen om de studie rond stamcellen vanuit een volledig ander perspectief te bekijken. Men probeert niet langer om stamcellen buiten het lichaam op te kweken tot een injecteerbare massa. In plaats daarvan concentreert men zich nu in de eerste plaats op de normale stamcelbiologie die hen drijft tot de vorming van nieuwe cellen in een orgaan. Als men de stamcellen in het beenmerg beschouwt, ziet men dat deze cellen af en toe migreren naar de bloedbaan, om zich vervolgens in een weefsel te nestelen en zich daar te integreren. Dit gebeurt voornamelijk wanneer het desbetreffende weefsel beschadigd is en is afhankelijk van een groot aantal regulatoren. Deze mechanismen kunnen door de mens gestimuleerd worden om zo meer stamcellen in de bloedbaan te krijgen, of om een betere aanhechting van stamcellen, bijvoorbeeld aan het hart, te verkrijgen. Hierbij moeten de stamcellen niet eerst uit het lichaam worden gehaald om ze dan weer te injecteren en kan men gebruikmaken van (relatief) gekende pathways.
Wetenschappers die zulk onderzoek verrichten, worden geconfronteerd met het probleem dat de cellen waarmee geëxperimenteerd wordt vaak afkomstig zijn van proefdieren.
Regulerende Factoren in Stamcelmigratie
Zowel adenosinetrifosfaat (ATP) als uridinetrifosfaat (UTP) zijn mediatoren die invloed hebben op de proliferatie, migratie en overlevingskansen van getransplanteerde stamcellen. De hepatocyte growth factor (HGF) is een cytokine dat voornamelijk wordt gevormd door mesenchymatische stamcellen. Het is betrokken bij de migratie, proliferatie en overleving van vele celtypen, waaronder beenmergstamcellen.
Sfingofosfolipiden zijn afgeleid van sfingosine en vormen een belangrijk onderdeel van de celmembraan. Zowel sfingosine als de geacetyleerde vorm, ceramide, zijn mogelijke precursoren voor respectievelijk sfingosine-1-fosfaat (S1P) en ceraminde-1-fosfaat (C1P).
Transforming growth factor-β (TGF-β) is een cytokine dat een rol speelt in immuniteit, migratie van stamcellen, proliferatie en hypertrofie. Ook bij weefselbeschadiging speelt TGF-β een rol. Wanneer endotheelcellen TGF-β in de extracellulaire matrix secerneren, bevindt het zich in een geïnactiveerde vorm. Bij weefselbeschadiging of inflammatie wordt deze vorm geactiveerd, waardoor TGF-β zijn werking kan uitoefenen. Deze geactiveerde vorm wordt dus ook uit endotheel vrijgesteld na beschadiging, en helpt in de migratie van stamcellen naar deze site.
De Stromale Cell-Derived factor-1 (SDF-1) grijpt aan op cellen met een CXCR4-receptor en reguleert een verscheidenheid aan fysiologische processen in de cel, zowel in normaal als in aangetast weefsel. De meeste effecten van SDF-1 zijn te verklaren door inductie van motiliteit, chemotaxis, adhesie. Wanneer de concentratie van SDF-1 op een plaats in het lichaam hoger wordt dan een vooropgestelde drempel, zullen de stamcellen in het beenmerg gestimuleerd worden om te migreren en te integreren op die plaats.
Wanneer de IGF-1 aan mesenchymatische stamcellen werd toegediend op de plaats van een hartinfarct, ziet men een vooruitgang in overleving en integratie in de gewenste zone. De groeifactor leidt tot een paracriene vrijstelling van SDF-1, waardoor er een migratiestroom ontstaat. SDF-1 is in staat om de stamcellen correct in het weefsel te integreren, wat leidt tot een verbetering van de hartfunctie.
Weefselbanken en Toekomstige Therapieën
Als de stamceltherapie op punt staat, is het aanleggen van een weefselbank met stamcellen uit navelstrengbloed van elk individu erg zinvol. Over de herkomst van de 'reserveonderdelen'.
Productie van embryo’s voor stamceltherapie. Het grote probleem is de vraag wanneer men kan spreken van menselijk leven. Tegenstanders van stamceltherapie, zoals christelijke bewegingen, beweren dat men van een individu kan spreken vanaf het ogenblik van bevruchting.
Een waardevoller alternatief bieden voor proefdieren of computersimulaties in de farmacologische industrie. Stamcellen kunnen gebruikt worden voor het modelleren van genetische ziekten. Ook kunnen op gecultiveerde stamcellijnen nieuwe geneesmiddelen worden getest om zo eventuele toxiciteit voortijdig op te sporen.
Sinds begin 2013 is het wetenschappers gelukt om humane stamcellen driedimensionaal te printen vanuit bio-inkt.
tags: #stamcellen #van #embryo #tegen #littekenweefsel